Nước – Wikipedia tiếng Việt

Nước là một hợp chất vô cơ, trong suốt, không vị, không mùi và gần như không màu, là thành phần chính của thủy quyển Trái đất và chất lỏng trong tất cả các sinh vật sống đã biết (trong đó nó hoạt động như một dung môi[5]). Nước rất quan trọng đối với tất cả các dạng sống đã biết, mặc dù nó không cung cấp calo hoặc chất dinh dưỡng hữu cơ. Công thức hóa học của nó là H2O, có nghĩa là mỗi phân tử của nó chứa một nguyên tử oxy và hai nguyên tử hydro, được nối với nhau bằng liên kết cộng hóa trị. Hai nguyên tử hydro liên kết với một nguyên tử oxy một góc 104,45°.[6]
” Nước ” là tên trạng thái lỏng của H2O ở điều kiện kèm theo tiêu chuẩn về nhiệt độ và áp suất. Nó tạo thành kết tủa dưới dạng mưa và sol khí dưới dạng sương mù. Mây gồm có những giọt nước và băng lơ lửng, ở trạng thái rắn. Khi được phân loại dạng mịn, nước đá kết tinh hoàn toàn có thể kết tủa dưới dạng tuyết. Trạng thái khí của nước là hơi nước .
Nước bao phủ 71% bề mặt Trái đất, chủ yếu ở các biển và đại dương.[7] Một phần nhỏ nước xuất hiện dưới dạng nước ngầm (1,7%), trong các sông băng và chỏm băng ở Nam Cực và Greenland (1,7%), và trong không khí dưới dạng hơi, mây (bao gồm băng và nước lỏng lơ lửng trong không khí) và giáng thủy (0,001%).[8][9] Nước di chuyển liên tục theo chu trình nước bốc hơi, thoát hơi nước, ngưng tụ, kết tủa và dòng chảy, thường là đi ra biển.
Bạn đang đọc: Nước – Wikipedia tiếng Việt
Nước đóng một vai trò quan trọng trong nền kinh tế tài chính quốc tế. Khoảng 70 % lượng nước ngọt mà con người sử dụng được dùng cho nông nghiệp. [ 10 ] Đánh bắt cá ở những vùng nước mặn và nước ngọt là nguồn cung ứng thực phẩm chính cho nhiều nơi trên quốc tế. Phần lớn thương mại đường dài của những sản phẩm & hàng hóa ( như dầu mỏ, khí đốt tự nhiên và những loại sản phẩm sản xuất ) được luân chuyển bằng thuyền qua những biển, sông, hồ và kênh đào. Một lượng lớn nước, đá và hơi nước được sử dụng để làm mát và sưởi ấm, trong công nghiệp và mái ấm gia đình. Nước là một dung môi tuyệt vời cho nhiều loại chất cả vô cơ và hữu cơ ; thế cho nên nó được sử dụng thoáng đãng trong những tiến trình công nghiệp, nấu ăn và giặt giũ. Nước, băng và tuyết cũng là TT của nhiều môn thể thao và những hình thức vui chơi khác, ví dụ điển hình như lượn lờ bơi lội, chèo thuyền vui chơi, đua thuyền, lướt sóng, câu cá thể thao, lặn, trượt băng và trượt tuyết .
Cấu tạo và đặc thù của phân tử nước[sửa|sửa mã nguồn]
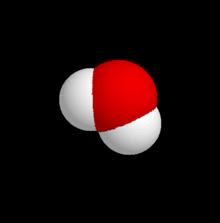 Mô hình phân tử nước
Mô hình phân tử nước
Hương vị và mùi[sửa|sửa mã nguồn]
Nước tinh khiết thường được diễn đạt là không vị và không mùi, mặc dầu con người có cảm ứng đặc biệt quan trọng hoàn toàn có thể cảm nhận được sự xuất hiện của nước trong miệng, và ếch được biết là có năng lực ngửi thấy nó. Tuy nhiên, nước từ những nguồn thường thì ( gồm có nước khoáng đóng chai ) thường có nhiều chất hòa tan, hoàn toàn có thể làm cho nó có nhiều mùi vị và mùi khác nhau. Con người và những động vật hoang dã khác đã tăng trưởng những giác quan cho phép họ nhìn nhận được chất lượng của nước bằng cách tránh nước quá mặn hoặc quá hôi .
Màu sắc và hình dáng[sửa|sửa mã nguồn]
Màu sắc tự nhiên của nước thường được xác lập bởi những chất rắn lơ lửng và chất lơ lửng, hoặc bằng cách phản chiếu khung trời, hơn là do nước. Điều này có nghĩa là sắc tố của nước phụ thuộc vào vào góc phản xạ và khúc xạ của ánh sáng chiếu đến .Ánh sáng trong phổ điện từ nhìn thấy hoàn toàn có thể đi qua một vài mét nước tinh khiết ( hoặc băng ) mà không có sự hấp thụ đáng kể, thế cho nên nó trông trong suốt và không màu. Như vậy thực vật thủy sinh, tảo, và sinh vật quang hợp khác hoàn toàn có thể sống trong nước sâu đến hàng trăm mét, chính do ánh sáng mặt trời hoàn toàn có thể tiếp cận chúng. Hơi nước cơ bản không nhìn thấy được như một chất khí .
Tuy nhiên, với độ dày 10 mét trở lên, màu sắc của nước (hoặc băng) là màu ngọc lam (màu xanh lục nhạt), vì phổ hấp thụ của nó có độ sắc nét tối thiểu ở màu tương ứng của ánh sáng (1/227 m −1 tại 418 nm). Màu sắc trở nên ngày càng mạnh mẽ và tối hơn với độ dày ngày càng tăng. (Thực tế không có ánh sáng mặt trời đến được các phần của đại dương dưới độ sâu 1000 mét) Mặt khác, tia cực tím bị nước hấp thụ mạnh. Và do thiếu ánh sáng và áp lực vô cùng lớn, như Rãnh Mariana, hơn
1
×
10
8
{\displaystyle 1\times 10^{8}}

N
/
m
2
{\displaystyle N/m^{2}}

Các chỉ số khúc xạ của nước lỏng ( 1.333 ở 20 °C ) là cao hơn nhiều so với không khí ( 1.0 ), tựa như như của alkan và ethanol, nhưng thấp hơn so với glycerol ( 1,473 ), benzen ( 1,501 ), carbon disulfide ( 1.627 ), và những loại kính thông dụng ( 1.4 đến 1.6 ). Chỉ số khúc xạ của băng ( 1.31 ) thấp hơn lượng nước .Nước không có hình dạng nhất định, nó chỉ sống sót hình dạng tại một thời gian trong vật mà nó chứa. Nó có cấu trúc phân tử chuyển dời trượt lên nhau và do đó nước rất dễ mất hình dạng, tuy nhiên nước rất khó nén, tận dụng đặc thù này, người ta vận dụng nguyên tắc Pascal cho những máy nén thủy lực .Xem thêm : Định luật Pascal
Hình học của phân tử nước[sửa|sửa mã nguồn]
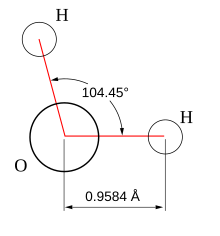
Phân tử nước gồm có hai nguyên tử hydrogen và một nguyên tử oxygen. Về mặt hình học thì phân tử nước có góc link là 104,45 °. Do những cặp điện tử tự do chiếm nhiều chỗ nên góc này rơi lệch đi so với góc lý tưởng của hình tứ diện. Chiều dài của link O-H là 95,84 picômét .
Tính lưỡng cực[sửa|sửa mã nguồn]
 Tính lưỡng cựcOxygen có độ âm điện cao hơn hydrogen. Việc cấu trúc thành hình ba góc và việc tích điện từng phần khác nhau của những nguyên tử đã dẫn đến cực tính dương ở những nguyên tử hydrogen và cực tính âm ở nguyên tử oxygen, gây ra sự lưỡng cực. Dựa trên hai cặp điện tử đơn độc của nguyên tử oxygen, kim chỉ nan VSEPR đã lý giải sự sắp xếp thành góc của hai nguyên tử hydrogen, việc tạo thành moment lưỡng cực và vì thế mà nước có những đặc thù đặc biệt quan trọng. Vì phân tử nước có tích điện từng phần khác nhau nên 1 số ít sóng điện từ nhất định như sóng cực ngắn có năng lực làm cho những phân tử nước xê dịch, dẫn đến việc nước được đun nóng. Hiện tượng này được vận dụng để sản xuất lò vi sóng .
Tính lưỡng cựcOxygen có độ âm điện cao hơn hydrogen. Việc cấu trúc thành hình ba góc và việc tích điện từng phần khác nhau của những nguyên tử đã dẫn đến cực tính dương ở những nguyên tử hydrogen và cực tính âm ở nguyên tử oxygen, gây ra sự lưỡng cực. Dựa trên hai cặp điện tử đơn độc của nguyên tử oxygen, kim chỉ nan VSEPR đã lý giải sự sắp xếp thành góc của hai nguyên tử hydrogen, việc tạo thành moment lưỡng cực và vì thế mà nước có những đặc thù đặc biệt quan trọng. Vì phân tử nước có tích điện từng phần khác nhau nên 1 số ít sóng điện từ nhất định như sóng cực ngắn có năng lực làm cho những phân tử nước xê dịch, dẫn đến việc nước được đun nóng. Hiện tượng này được vận dụng để sản xuất lò vi sóng .
Liên kết hiđrô[sửa|sửa mã nguồn]
Các phân tử nước tương tác lẫn nhau trải qua link hydrogen và nhờ vậy có lực hút phân tử lớn. Đây không phải là một link bền vững và kiên cố. Liên kết của những phân tử nước trải qua link hiđrô chỉ sống sót trong một phần nhỏ của một giây, sau đó những phân tử nước tách ra khỏi link này và link với những phân tử nước khác .
 Phân tử nướcĐường kính nhỏ của nguyên tử hydrogen đóng vai trò quan trọng cho việc tạo thành những link hydrogen, do tại chỉ có như vậy nguyên tử hydrogen mới hoàn toàn có thể đến gần nguyên tử oxygen một chừng mực khá đầy đủ. Các chất tương tự của nước, Ví dụ như acid sulfuric ( H2S ), không tạo thành những link tựa như vì hiệu số điện tích quá nhỏ giữa những phần link. Việc tạo chuỗi của những phân tử nước trải qua link cầu nối hydrogen là nguyên do cho nhiều đặc thù đặc biệt quan trọng của nước, ví dụ như nước mặc dầu có khối lượng mol nhỏ vào lúc 18 g / mol vẫn ở thể lỏng trong điều kiện kèm theo tiêu chuẩn. Ngược lại, H2S sống sót ở dạng khí cùng ở trong những điều kiện kèm theo này. Nước có khối lượng riêng lớn nhất ở 4 độ Celcius và nhờ vào đó mà băng đá hoàn toàn có thể nổi lên trên mặt nước ; hiện tượng kỳ lạ này được lý giải nhờ vào link cầu nối hiđrô .
Phân tử nướcĐường kính nhỏ của nguyên tử hydrogen đóng vai trò quan trọng cho việc tạo thành những link hydrogen, do tại chỉ có như vậy nguyên tử hydrogen mới hoàn toàn có thể đến gần nguyên tử oxygen một chừng mực khá đầy đủ. Các chất tương tự của nước, Ví dụ như acid sulfuric ( H2S ), không tạo thành những link tựa như vì hiệu số điện tích quá nhỏ giữa những phần link. Việc tạo chuỗi của những phân tử nước trải qua link cầu nối hydrogen là nguyên do cho nhiều đặc thù đặc biệt quan trọng của nước, ví dụ như nước mặc dầu có khối lượng mol nhỏ vào lúc 18 g / mol vẫn ở thể lỏng trong điều kiện kèm theo tiêu chuẩn. Ngược lại, H2S sống sót ở dạng khí cùng ở trong những điều kiện kèm theo này. Nước có khối lượng riêng lớn nhất ở 4 độ Celcius và nhờ vào đó mà băng đá hoàn toàn có thể nổi lên trên mặt nước ; hiện tượng kỳ lạ này được lý giải nhờ vào link cầu nối hiđrô .
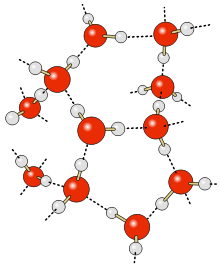 Liên kết hiđrô
Liên kết hiđrô
Các đặc thù hóa lý của nước[sửa|sửa mã nguồn]
Cấu tạo của phân tử nước tạo nên những link hiđrô giữa những phân tử là cơ sở cho nhiều đặc thù của nước. Cho đến nay 1 số ít đặc thù của nước vẫn còn là câu đố cho những nhà nghiên cứu mặc dầu nước đã được nghiên cứu và điều tra từ lâu .
Nhiệt độ nóng chảy và nhiệt độ sôi của nước đã được Anders Celsius dùng làm hai điểm mốc cho độ bách phân Celcius. Cụ thể, nhiệt độ đóng băng của nước là 0 độ Celcius, còn nhiệt độ sôi (760 mmHg) bằng 100 độ Celcius. Nước đóng băng được gọi là nước đá. Nước đã hóa hơi được gọi là hơi nước. Nước có nhiệt độ sôi tương đối cao nhờ liên kết hiđrô.
Dưới áp suất thông thường nước có khối lượng riêng ( tỷ trọng ) cao nhất là ở 4 °C : 1 g / cm ³ đó là vì nước vẫn liên tục co và giãn khi nhiệt độ giảm xuống dưới 4 °C. Điều này không được quan sát ở bất kể một chất nào khác. Điều này có nghĩa là : Với nhiệt độ trên 4 °C, nước có đặc tính giống mọi vật khác là nóng nở, lạnh co ; nhưng với nhiệt độ dưới 4 °C, nước lại lạnh nở, nóng co. Do hình thể đặc biệt quan trọng của phân tử nước ( với góc link 104,45 ° ), khi bị làm lạnh những phân tử phải dời xa ra để tạo link tinh thể lục giác mở. Vì vậy mà tỉ trọng của nước đá nhẹ hơn nước thể lỏng. [ 11 ]
 Khi ướp đông dưới 4 °C, những phân tử nước phải dời xa ra để tạo link tinh thể lục giác mở .
Khi ướp đông dưới 4 °C, những phân tử nước phải dời xa ra để tạo link tinh thể lục giác mở .
Nước là một dung môi tốt nhờ vào tính lưỡng cực. Các hợp chất phân cực hoặc có tính ion như acid, rượu và muối đều dễ tan trong nước. Tính hòa tan của nước đóng vai trò rất quan trọng trong sinh học vì nhiều phản ứng hóa sinh chỉ xảy ra trong dung dịch nước.
Nước tinh khiết không dẫn điện. Mặc dù vậy, do có tính hòa tan tốt, nước hay có tạp chất pha lẫn, thường là những muối, tạo ra những ion tự do trong dung dịch nước được cho phép dòng điện chạy qua .Về mặt hóa học, nước là một chất lưỡng tính, hoàn toàn có thể phản ứng như một, hoàn toàn có thể hiểu đơn thuần khi một oxide acid hoặc một oxide base tính năng với nước sẽ tạo ra dung dịch acid hay base tương ứng. Ở 7 pH ( trung tính ) hàm lượng những ion hydroxyt ( OH – ) cân đối với hàm lượng của hydronium ( H3O + ). Khi phản ứng với một axit mạnh hơn ví dụ như HCl, nước phản ứng như một chất kiềm :
- HCl + H2O ↔ H3O+ + Cl-
Với ammoniac nước lại phản ứng như một axit :
- NH3 + H2O ↔ NH4+ + OH-
Trong công nghiệp[sửa|sửa mã nguồn]
Trong công nghiệp, nước hoàn toàn có thể hóa lỏng bằng cách làm tan băng đá, hoặc lọc từ nước biển và những nguồn nước không tinh khiết bằng những giải pháp khác nhau như lọc, chiết, tách, chưng cất ( Chưng cất là một giải pháp tách dùng nhiệt để tách hỗn hợp đồng thể của những chất lỏng khác nhau. Chất rắn hòa tan, ví dụ như những loại muối, được tách ra khỏi chất lỏng bằng cách kết tinh. Dung dịch muối hoàn toàn có thể làm cô đặc bằng cách cho bay hơi ), bốc hơi nước, … có sự phối hợp của ngưng tụ .
Trong phòng thí nghiệm[sửa|sửa mã nguồn]
Chủ yếu người ta dùng cách cho
H
2
{\displaystyle {\ce {H2}}}

O
2
{\displaystyle {\ce {O2}}}

2
H
2
+
O
2
→
t
e
m
p
e
r
a
t
u
r
e
2
H
2
O
{\displaystyle {\ce {2H2 + O2 ->[temperature] 2H2O}}}
[sửa|sửa mã nguồn]
Hiện nay nguồn nước mà người dân sử dụng trong hoạt động và sinh hoạt hàng ngày thường được lấy từ : Hệ thống phân phối nước tập trung chuyên sâu ( nước máy ), nước mưa, nước giếng khơi, nước máng lần, nước giếng khoan …
Nước trong đời sống[sửa|sửa mã nguồn]
Sự sống trên Trái Đất bắt nguồn từ trong nước. Tất cả những dạng sống trên Trái Đất đều nhờ vào vào nước và vòng tuần hoàn nước .Nước có ảnh hưởng tác động quyết định hành động đến khí hậu và là nguyên do tạo ra thời tiết. Năng lượng mặt trời sưởi ấm không đồng đều những đại dương đã tạo nên những dòng hải lưu trên toàn thế giới. Dòng hải lưu Gulf Stream luân chuyển nước ấm từ vùng Vịnh Mexico đến Bắc Đại Tây Dương làm tác động ảnh hưởng đến khí hậu của vài vùng châu Âu .Nước là thành phần quan trọng của những tế bào sinh học và là môi trường tự nhiên của những quy trình sinh hóa cơ bản như quang hợp .Hơn 75 % diện tích quy hoạnh của Trái Đất được bao trùm bởi nước. Lượng nước trên Trái Đất có vào lúc 1,38 tỉ km³. Trong đó 97,4 % là nước mặn trong những đại dương trên quốc tế, phần còn lại, 2,6 %, là nước ngọt, sống sót hầu hết dưới dạng băng tuyết đóng ở hai cực và trên những ngọn núi, chỉ có 0,3 % nước trên toàn quốc tế ( hay 3,6 triệu km³ ) là hoàn toàn có thể sử dụng làm nước uống. Việc cung ứng nước uống sẽ là một trong những thử thách lớn nhất của loài người trong vài thập niên tới đây. Nguồn nước cũng đã là nguyên do gây ra một trong những cuộc cuộc chiến tranh ở Trung Cận Đông .Nước được sử dụng trong công nghiệp từ lâu như là nguồn nguyên vật liệu ( cối xay nước, máy hơi nước, nhà máy sản xuất thủy điện ) như thể chất trao đổi nhiệt .Nhà triết học người Hy Lạp Empedocles đã coi nước là một trong bốn nguồn gốc tạo ra vật chất ( bên cạnh lửa, đất và không khí ). Nước cũng nằm trong Ngũ Hành của triết học cổ Trung Hoa .Với thực trạng ô nhiễm ngày một nặng và dân số ngày càng tăng, nước sạch dự báo sẽ sớm trở thành một thứ tài nguyên quý giá không kém dầu mỏ trong thế kỷ trước. Nhưng không như dầu mỏ hoàn toàn có thể sửa chữa thay thế bằng những loại nguyên vật liệu khác như điện, nguyên vật liệu sinh học, khí đốt …, nước không hề thay thế sửa chữa và trên quốc tế tổng thể những dân tộc bản địa đều cần đến nó để bảo vệ đời sống của mình, cho nên vì thế yếu tố nước trở thành chủ đề quan trọng trên những hội đàm quốc tế và những xích míc về nguồn nước đã được dự báo trong tương lai. Tuy nhiên gần đây người ta đã lọc được nước biển từ một thiết bị lọc rẻ tiền và từ đó xử lý được yếu tố thiếu nước .
- OA Jones, JN Lester and N Voulvoulis, Pharmaceuticals: a threat to drinking water? TRENDS in Biotechnology 23(4): 163, 2005
- Franks, F (Ed), Water, A comprehensive treatise, Plenum Press, New York, 1972-1982
- PH Gleick and associates, The World’s Water: The Biennial Report on Freshwater Resources. Island Press, Washington, D.C. (published every two years, beginning in 1998.)
- Marks, William E., The Holy Order of Water: Healing Earth’s Waters and Ourselves. Bell Pond Books (a div. of Steiner Books), Great Barrington, MA, November 2001 [ISBN 0-88010-483-X]
- Debenedetti, P. G., and Stanley, H. E.; “Supercooled and Glassy Water”, Physics Today 56 (6), p. 40-46 (2003). Downloadable PDF (1.9 MB)
Nước như một nguồn tài nguyên tự nhiên[sửa|sửa mã nguồn]
Liên kết ngoài[sửa|sửa mã nguồn]
Source: https://trangdahieuqua.com
Category: Làm đẹp



